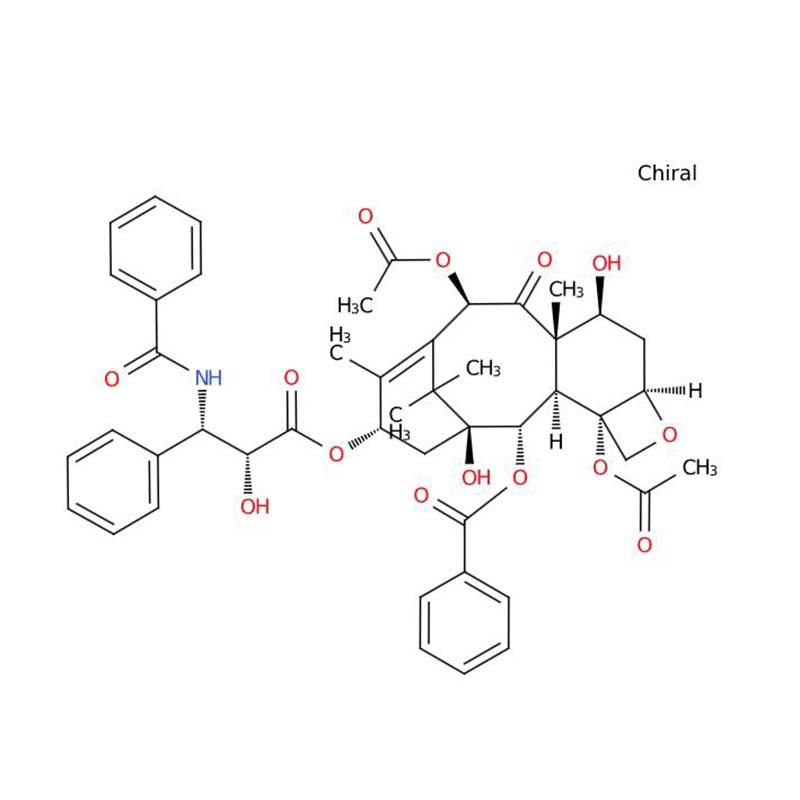
Паклитаксел CAS: 33069-62-4
Механизм действия:Этот терапевтический агент специфически прикрепляется к собранным микротрубочкам, способствуя их стабильности и тем самым препятствуя нормальным процессам деления клеток.
Онкологическая эффективность:Клинически доказанная эффективность против ряда видов рака, включая рак яичников, молочной железы, немелкоклеточный рак легких, колоректальный рак и другие солидные опухоли.
Нарушение клеточного цикла:Запускает остановку клеточного цикла именно во время митоза, тем самым подавляя пролиферацию злокачественных клеток и рост опухоли.
Клинические данные:Широко используется в передовых схемах лечения рака, надежные данные об эффективности подтверждены клиническими исследованиями фазы II и фазы III.
Обзор продукта
Паклитаксел — это дитерпеновое соединение, первоначально извлеченное из коры Taxus brevifolia (типа Тихоокеанский тис). Будучи представителем группы таксановых противоопухолевых препаратов, он стал одним из наиболее ценных с клинической точки зрения и широко применяемых химиотерапевтических препаратов в современной онкологии.
Его молекулярная формула — C₄₇H₅₁NO₁₄, регистрационный номер в системе CAS — 33069-62-4, а молекулярная масса — 853,9 г/моль. Паклитаксел представляет собой белый или почти белый кристаллический порошок с высокой липофильностью и низкой водорастворимостью.
Паклитаксел является основным компонентом стандартных схем химиотерапии и широко используется для лечения различных солидных опухолей, а также включен в Модельный список основных лекарственных средств ВОЗ.
2. Ключевые особенности
Уникальное действие, стабилизирующее микротрубочки: В отличие от традиционных антимитотических препаратов, которые подавляют образование микротрубочек, паклитаксел активно способствует полимеризации микротрубочек и усиливает структурную стабильность, тем самым блокируя динамический баланс, необходимый для митоза.
Широкий противоопухолевой спектр действия: Он демонстрирует значительное ингибирующее действие против рака яичников, рака молочной железы, рака легких и связанной с СПИДом саркомы Капоши, а также обладает терапевтическим потенциалом против многих других злокачественных опухолей.
Вмешательство в клеточный цикл на различных стадиях: Агент в основном останавливает пролиферацию клеток на поздних фазах G2 и M; кроме того, он может воздействовать на интерфазные клетки, разрушая связь между ядром и цитоскелетом.
Индукция различных путей гибели клеток: Паклитаксел может активировать несколько программируемых механизмов клеточной гибели, включая апоптоз, пироптоз, ферроптоз и некроптоз, которые в совокупности усиливают его противоопухолевое действие.
Доказанная клиническая ценность: Подтвержденные многолетним клиническим применением и обширными исследованиями, его схема дозирования, профиль безопасности и комбинированные терапевтические стратегии были полностью разработаны и стандартизированы.
Разнообразные лекарственные формы: В дополнение к классическому препарату на основе кремофора EL, существуют усовершенствованные формулы, такие как паклитаксел, связанный с альбумином (Абраксан). ® ) были разработаны для уменьшения негативных реакций, связанных с использованием растворителей.
Расширенные возможности применения в интервенционных устройствах: За пределами области терапии рака, баллоны и стенты, высвобождающие паклитаксел, широко используются при лечении периферического артериального заболевания (ПАД) для предотвращения сосудистого рестеноза.
3. Технические характеристики с пояснениями
| Параметр | Типичное значение/характеристика | Описание и значение |
|---|---|---|
| Номер CAS | 33069-62-4 | Универсальный химический идентификатор |
| Молекулярная формула | C₄₇H₅₁NO₁₄ | Сложная дитерпеновая структура с системой таксановых кольцевых соединений |
| Молекулярная масса | 853,9 г/моль | Используется для стоициометрических расчетов и составления формул. |
| Внешний вид | Белый или почти белый кристаллический порошок | Визуальный индикатор качества |
| Температура плавления | 213-216 ° C (разлагается) | Характерная физическая величина |
| Растворимость | Вода: Практически нерастворима Этанол: Растворимый Органические растворители: растворимы в ДМСО,метанолацетонитрил |
Высокая липофильность требует использования солюбилизаторов (Cremophor EL) или современных формул. |
| Коэффициент разделения (лог P) | 3.0 | Высокая липофильность влияет на распределение и связывание с белками. |
| Связывание с белком | 89% | В значительной степени связан с плазменными белками. |
| Метаболизм | Печеночная пассажирка через CYP2C8 и CYP3A4 | Основной путь элиминации; потенциал взаимодействия лекарств. |
| Хаф-Лайф | 9,9 часа (3-часовая инфузия) | Нелинейная фармакокинетика; зависит от дозы и схемы приема. |
| Устранение | 71% фекалий (120 часов, 5% неизменено) 1,3-12,7% в моче в виде неизмененного препарата |
В основном экскретируется через желчевыводящие протоки. |
| Преодоление гематоэнцефалического барьера | Нет | Ограниченное проникновение в центральную нервную систему |
4. Приложения
Онкологические показания
Основные лицензированные терапевтические показания
Рак яичников: Используется в качестве средства первой линии в сочетании с цисплатином при распространенной карциноме яичников, а также применяется в качестве средства второй линии при метастатических поражениях.
Рак молочной железы: Применяется в качестве адъювантной терапии при лимфоузловой интрузии рака молочной железы после схем лечения на основе доксорубицина; также используется для лечения метастатических случаев, не поддающихся комбинированной химиотерапии, или случаев рецидива в течение шести месяцев после адъювантного лечения.
Немелкоклеточный рак легких (НМКЛ): применяется в комбинации с цисплатином в качестве терапии первой линии для пациентов, которым не подходит радикальная хирургическая резекция или лучевая терапия.
Саркома Капоши, связанная с СПИДом:Рекомендуется в качестве терапевтического средства второго ряда.
Применение за пределами стандартных показаний и в соответствии с рекомендациями.
Интервенционная кардиология и сосудистая хирургия
Стенты с паклитакселом обеспечивают непрерывное и стабильное высвобождение препарата, что способствует сохранению длительной проходимости артерии после процедуры имплантации стента.
5. Состав и сравнение продуктов
| Параметр | Обычный паклитаксел | Паклитаксел, связанный с альбумином (Абраксан) ® ) |
|---|---|---|
| Формулировка | Кремофор EL (полиоксиэтилированное касторовое масло) + этанол | Наночастицы, связанные с альбумином |
| Концентрация | 6 мг/мл | Лиофилизированный порошок для восстановления. |
| Администрация | Внутривенная инфузия в течение 1-24 часов с встроенным фильтром | Внутривенная инфузия в течение 30 минут, фильтр не требуется. |
| Препарационная терапия | Требуется: АссистентДексаметазон + антигистаминные препараты + антагонисты H2-рецепторов для предотвращения гиперчувствительности | Не требуется для предотвращения гиперчувствительности. |
| Дозирование | 135-175 мг/м² каждые 3 недели; доступны еженедельные схемы приема. | 260 мг/м² каждые 3 недели (грудь); 100 мг/м² еженедельно (НСЛК, поджелудочная железа) |
| Ключевое преимущество | Десятилетия клинического опыта, хорошо изученные. | Устраняет токсические эффекты, связанные с кремофолом, более высокая допустимая доза, не требует предварительной премедикации. |
| Основные показания | Овариальная раковая опухоль, рак молочной железы, несахаридодермальный рак легких, саркома Капоши | Грудь, несоответствующий клеточному типу рака легких, аденокарцинома поджелудочной железы |
6. Руководство по дозировке и применению
Стандартные схемы дозирования
| Индикация | Режим | График дозирования |
|---|---|---|
| Рак яичников | 135-175 мг/м² внутривенно | Каждые 3 недели (с цисплатином) |
| Рак молочной железы | 175 мг/м² внутривенно | Каждые 3 недели |
| НСКЛК | 135 мг/м² внутривенно | Каждые 3 недели (с цисплатином) |
| Саркома Капоши | 135 мг/м² внутривенно | Каждые 3 недели; или 100 мг/м² каждые 2 недели |
| Еженедельный режим | 80-100 мг/м² внутривенно | Еженедельно (различные солидные опухоли) |
Требования к предварительной медикаментозной обработке
Стандартный 3-недельный курс подготовительных препаратов:
Дексаметазон 20 мг перорально за 12 и 6 часов до приема пищи ИЛИ 20 мг внутривенно за 30 минут до приема пищи.
Дифенгидрамин 25-50 мг внутривенно/перорально за 30-60 минут до начала лечения.
Ранитидин 50 мг внутривенно или фамотидин 20 мг внутривенно за 30-60 минут до начала лечения.
Еженедельный режим перед тренировкой (за 30-60 минут до начала):
Дексаметазон 10 мг внутривенно
Дифенгидрамин 25-50 мг внутривенно/перорально
Ранитидин 50 мг внутривенно или фамотидин 20 мг внутривенно
Корректировка дозировки в связи с токсичностью
| Токсичность | Рекомендуемое действие |
|---|---|
| Фебрильная нейтропения | Снизить дозу на 20%. |
| Нейтропения 4 степени (≥5-7 дней) | Снизить дозу на 20%. |
| Тромбоцитопению 4 степени | Снизить дозу на 20%. |
| Нейротоксичность 3-го степени | Снизить дозу на 20%. |
| Нейротоксичность 4-го степени | Прекратить |
| Кистоидный макулярный отек (любой степени тяжести) | Прекратить |
Требования к администрированию
Разбавление: Необходимо разбавить перед внутривенной инфузией.
Фильтрация: Подавать через встроенный фильтр ≤0,22 мкм
Последовательность: При сочетании с соединениями платины сначала вводят паклитаксел.
Стабильность инфузионного раствора: 27 часов при комнатной температуре (25 ° в) при естественном освещении
Хранение: Храните флаконы в оригинальной упаковке при температуре 15-30 градусов. ° C, защищено от света
7. Профиль безопасности и переносимости
Противопоказания
Сильная гиперчувствительность к паклитакселу или полиоксиэтилированному касторовому маслу (Кремофор EL).
Начальный уровень нейтрофилов < 1500 клеток/мм³ (средственные опухоли)
Начальный уровень нейтрофилов < 1000 клеток/мм³ (саркома Капоши, связанная с СПИДом)
Беременность (категория D)
Наиболее распространенные побочные эффекты
| Неблагоприятный эффект | Частота случаев | Характеристики |
|---|---|---|
| Алоpecia | 93% | Редко бывает постоянным |
| Периферическая невропатия | 64% (тяжелый 4%) | Зависит от дозы и накопительного эффекта; проявляется в виде онемения, покалывания, жгучей боли в области перчаток и носков; обычно улучшается/исчезает через несколько месяцев после лечения. |
| Боль в опорно-двигательном аппарате | 54% (тяжелый 12%) | Появляется через 2-3 дня после приема, исчезает в течение нескольких дней; Нестероидные противовоспалительные препараты эффективны. |
| Дискомфорт/Рвота | 44% | Низкий эметогенный потенциал |
| Гиперчувствительность | 40% (тяжелый 1%) | Проявляется на ранних стадиях, в течение первого часа после инфузии; предотвращается с помощью премедикации. |
| Диарея | 25% | Может быть серьезным |
| Отек | 21% | |
| Усталость | 17% | |
| Миелопрессура | Нейтропения 4-го степени 27% | Зависит от дозы и графика приема; не накапливается. |
Серьезные неблагоприятные события [цитата]
| Событие | Заметки |
|---|---|
| Анафилаксис | 2% пациентов; может привести к смерти |
| Сердечно-сосудистая система | Гипотония (11%), аритмия (3%), брадикардия (обычно бессимптомная) |
| Периферическая невропатия | Может ограничивать дозировку; легкие симптомы обычно обратимы. |
| Кистоидный макулярный отек | Редкость; обратимость после прекращения действия. |
| Интерстициальный пневмонит | Редкий |
| Воспоминания о радиации | Усиленное радиационное повреждение тканей; может возникнуть через несколько недель или месяцев после облучения. |
Особые группы населения
Пациенты с ВИЧ: Токсичность может быть более выраженной, особенно фебрильная нейтропения и инфекции.
Предыстория воздействия антациклинов: сообщалось о риске застойной сердечной недостаточности (включая снижение левого изотонического давления).
8. Нормативный статус и разрешения
Глобальные регуляторные одобрения
| Регион/Страна | Одобренные показания | Идентификатор |
|---|---|---|
| Соединенные Штаты (FDA) | Овариальная раковая опухоль, рак молочной железы, несахаридодермальный рак легких, саркома Капоши | НДА 020262 |
| Европейский Союз (ЕС) | Овариальная раковая опухоль, рак молочной железы, несахаридодермальный рак легких, саркома Капоши | ЕМЕА/Х/С/000259 |
| Саудовская Аравия (SFDA) | Овариальная раковая опухоль, рак молочной железы, несахаридодермальный рак легких, саркома Капоши | Паклитаксел Каби, 6 мг/мл |
| Тайвань | Овариальная раковая опухоль, рак молочной железы, несахаридодермальный рак легких, саркома Капоши | BB21157221 (Таксол) ® ) |
| Япония (PMDA) | Множественные солидные опухоли |
Ключевые нормативные положения
Применение медицинских устройств:
Катетеры и стенты, покрытые паклитакселом, используемые для лечения периферического артериального заболевания (ПАД), классифицируются и регулируются как медицинские изделия. Управление по санитарному надзору за продуктами и лекарствами США (FDA) провело всестороннюю оценку соответствующих данных по безопасности и пришло к выводу, что имеющиеся данные не указывают на повышенный риск смертности, связанный с этими устройствами.
Постмаркетинговый надзор за безопасностью:
В 2019 году проведённый FDA метаанализ первоначально выявил потенциальный сигнал задержки смертности, связанной с устройствами, покрытыми паклитакселом. Однако последующие долгосрочные исследования, включая исследование SWEDEPAD, исследование VOYAGER PAD и обновленные метаанализы рандомизированных контролируемых исследований (РКИ), не смогли подтвердить этот риск. FDA продолжает рекомендовать стандартное клиническое наблюдение пациентов и всестороннее информирование о преимуществах и рисках перед началом лечения.
9. Лекарственное взаимодействие
Основные метаболические взаимодействия
| Класс/вид лекарственного препарата | Эффект | Клиническое значение |
|---|---|---|
| Ингибиторы CYP2C8 (гемфиброзил и др.) | Может увеличить экспозицию паклитакселу | Контролировать повышение токсичности |
| Ингибиторы CYP3A4 (кетоконазол, эритромицин и т.д.) | Может увеличить экспозицию паклитакселу | Контролировать повышение токсичности |
| Индукторы CYP2C8/3A4 (рифампин, карбамазепин и т.д.) | Может снизить экспозицию паклитакселу | Возможность снижения эффективности |
Взаимодействия, зависящие от последовательности действий
Цисплатин/Карбоплатин: Сначала вводите паклитаксел для минимизации миелосупрессии.
Доксорубицин: вводите паклитаксел после доксорубицина, чтобы избежать снижения клиренса доксорубицина.
10. Доставка, Сертификация и Обслуживание
Информация о цепочке поставок
Источники API: Множество квалифицированных производителей по всему миру
Готовый продукт: доступен в форме флаконов по 30 мг/5 мл, 100 мг/16,7 мл, 300 мг/50 мл (стандартная); лиофилизированный порошок для формулировки, связанной с альбумином.
Требования к хранению: 15-30 ° C, хранить в темном месте.
Срок годности: обычно 24-36 месяцев при правильных условиях хранения.
Сертификаты качества
Сертификат анализа (COA) предоставляется к каждой партии.
Паспорт безопасности (SDS) доступен на нескольких языках.
Спецификация продукта (PS), документирующая чистоту, идентичность и концентрацию.
Сертификат происхождения (COO) предоставляется по запросу.
Наличие нормативной документации
Доступ к базе данных Drug Master File (DMF) для производителей фармацевтической продукции
Документация по соответствию требованиям GMP
Заявления о соответствии требованиям REACH/TSCA
Экспортная документация для международных перевозок